
МЕДИЦИНСКОЙ ПРОМЫШЛЕННОСТИ
О мерах по координации усилий государства и бизнеса в целях развития фармацевтической и медицинской промышленности и достижения технологического суверенитета
Обсудив отчетный доклад Всероссийского общественного совета фармацевтической и медицинской промышленности (Ю.Т. Калинин, В.А. Дмитриев, А.Д. Апазов, И.В. Ожгихин, В.В. Колин, А.Ю. Герштейн, О.А. Пелехатая, А.Л. Кедрин, Л.В. Титова, Н.К. Дараган, А.Р.Дабагов) о работе по повышению конкурентоспособности производства медицинской продукции, обеспечения лекарственной независимости и безопасности Российской Федерации, приоритетов национального проекта здравоохранения, и выступления Министра здравоохранения РФ М.А.Мурашко, заместителя Министра промышленности и торговли РФ Е.Г.Приезжевой, Президента ТПП РФ С.Н.Катырина, первого заместителя Председателя Комитета Государственной Думы Т.В.Буцкой, члена Комитета Совета Федерации по социальной политике М.В.Левиной, Вице-Президент РСПП В.М.Черепова, Члена Президиума, академика-секретаря Отделения медицинских наук РАН В.И.Стародубова, заместителя Руководителя Росздравнадзора Д.Ю.Павлюкова, директора Департамента регулирования обращения лекарственных средств и медицинских изделий Минздрава России Е.М.Астапенко, врио директора Департамента развития фармацевтической и медицинской промышленности Минпромторга России Е.А.Шикиной, директора Департамента радиоэлектронной промышленности Ю.В.Плясунова,. заместителя директора Департамента развития фармацевтической и медицинской промышленности Минпромторга России О.Г.Кравцовой, ректора Санкт-Петербургского государственного химико-фармацевтического университета И.А.Наркевича, генерального директора ФГБУ «Научный центр экспертизы средств медицинского применения» Минздрава России В.В.Косенко, директора Департамента ФГАОУ ВО Первого МГМУ имени И.М.Сеченова Е.И.Парамоновой, руководителя юридического отдела АО «Активный компонент» М.Ю.Комаровой, руководителя секретариата Департамента технического регулирования ЕЭК Д.А.Щекина, съезд отметил:
1. В отчетный период Всероссийский совет фармацевтической и медицинской промышленности осуществлял свою деятельность в условиях применения по отношению Российской Федерации жестких ограничительных мер экономического характера и резкого колебания курса рубля. Положение осложнялось высокой зависимостью производства лекарственных средств и медицинских изделий от импорта оборудования, сырья, материалов и комплектующих, применяемых в технологиях их получения, а также несовершенством системы нормативного правового регулирования обращения продукции.
Разработанный согласно постановления 14 съезда план мероприятий по его реализации предусматривал организацию работ по:
- созданию инновационных лекарственных средств и медицинских изделий как замещающих импорт, так и оригинальных;
- развитию производства фармацевтических субстанций;
- созданию производства продукции малотоннажных химических веществ и полимерных материалов для нужд фармацевтической и медицинской промышленности;
- совершенствованию государственной регистрации лекарственных средств и медицинских изделий по национальным правилам и правилам ЕАЭС;
- совершенствованию системы государственных закупок медицинской продукции;
- разработке приоритетных направлений развития фармацевтической и медицинской промышленности;
- разработке нормативных документов, регулирующих подтверждение производства промышленной продукции на территории Российской Федерации, в связи с введением бальной оценки подтверждения;
- мерам государственной поддержки и стимулирования развития производства лекарственных средств и медицинских изделий.
Рассмотрению вопросов плана было посвящено 15 заседаний Президиума Всероссийского общественного совета, 7 круглых столов, организованных совместно профильными комиссиями и комитетами РСПП, ТПП РФ, Деловой России, Опоры России, Отделением медицинских наук и отделением химии и наук о материалах РАН. Позиция объединений по ним была представлена на круглом столе в Совете Федерации, на заседании Экспертного совета Государственной Думы, международного Военно-технического форума «Армия-2023», 25 ежегодной конференции «ФармМедОбращение-2023», VIII ежегодном форуме «Биотехмед», III Всероссийском форуме «NOVAMED-2023», ряде совещаний в федеральных органах исполнительной власти и на Стратегической сессии по развитию промышленности. Часть решений, принятых в ходе проведенных мероприятий, оформлены в виде ведомственных нормативных документов, постановлений Правительства РФ и изменений в законодательстве РФ, что во многом способствовало достижению стабильности в работе предприятий и, несмотря на отмеченные выше жесткие санкции экономического характера, предотвращению появления сколько-нибудь значительного количества дефектуры продукции и позволило значительно увеличить мощности Российской Федерации по производству лекарств и медицинской техники и в объемах, и в номенклатуре.
По итогам 2022 года объем производства лекарственных средств составил 607,9 млрд руб. (+10,6% к 2021г.), за 6 месяцев 2023г. – 310,6 млрд руб. Доля лекарств российского производства в объеме рынка составила 36,6% (61,8 в упаковках), а в перечне ЖНВЛП – 80%. При этом рост доли лекарств российского производства отмечается практически по всем фармакотерапевтическим группам и вакцинным препаратам, а также лекарствам, находящихся в перечнях высоко затратных назологий и стратегически значимых лекарственных средств, производство которых должно быть обеспечено на территории Российской Федерации. Российскими компаниями реализуются более 110 проектов по созданию, новых производственных мощностей и модернизации действующих с общем объемом инвестиций около 100 млрд руб. Продолжаются работы по продвижению лекарств на внешние рынки, объем экспорта фармацевтической продукции в 2022г. превысил 1,28 млрд долларов, а за 6 месяцев 2023г. – 0,39 млрд долларов.
Основные показатели фармацевтического рынка Российской Федерации.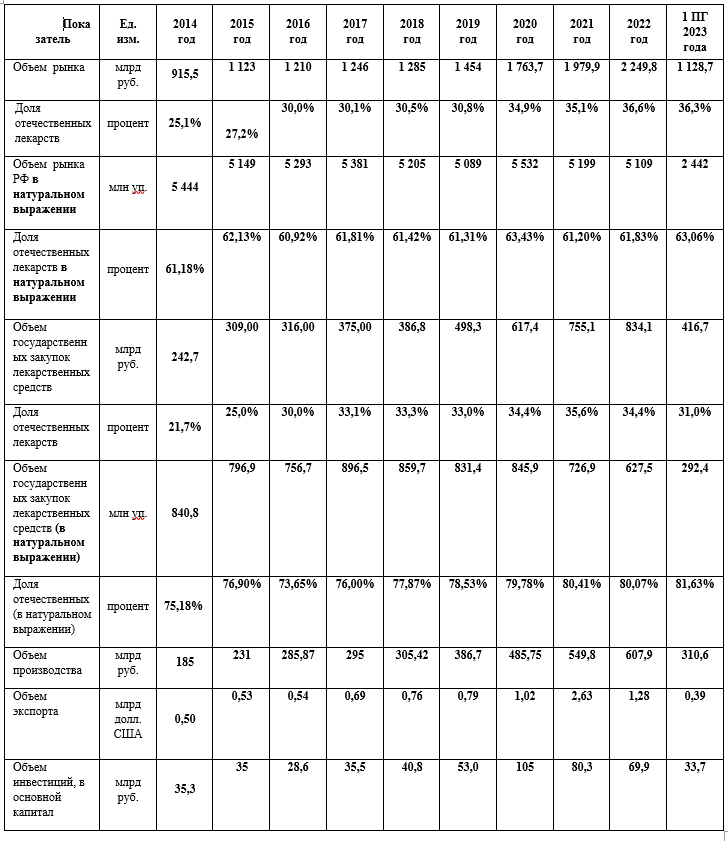
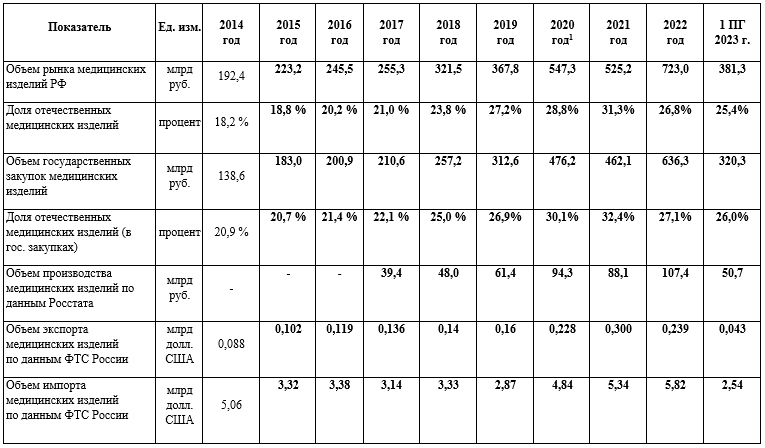
3. В рамках реализации реформы по совершенствованию контрольных (надзорных) и разрешительных функций органов исполнительной власти (регуляторная гильотина) рабочими группами от экспертного и делового сообщества в сфере фармацевтики и медицинских изделий и в сфере безопасности донорской крови при Правительственной Комиссии рассмотрено и согласовано более 50 проектов нормативных актов ведомственного, правительственного и законодательного уровней. По предложениям Союза ассоциаций и предприятий фармацевтической и медицинской промышленности:
- Минздрав России подготовил проект постановления о внесении изменений в правила государственной регистрации предельных отпускных цен производителей на препараты из перечня ЖНВЛП, касающиеся сокращения сроков предоставления услуги по регистрации с 60 до 43 дней, сокращения количества предоставляемых заявителем документов, уточнения механизма ценообразования на иммунобиологические лекарственные препараты и препараты из крови и др.
- Правительством РФ внесен в Государственную Думу проект закона о внесении изменений в Налоговый Кодекс в части налогообложения НДС медицинских изделий.
- Правительством РФ расширен перечень медицинских изделий, на которые распространяется запрет на допуск товаров, происходящих из иностранных государств, для целей осуществления закупок для государственных и муниципальных нужд.
- Внесены изменения в федеральный закон «Об обращении лекарственных средств» в части регулирования обращения в рамках ЕАЭС.
- Минздравом России внесены в Правительство РФ предложения о продлении сроков действия постановлений Правительства РФ от 23.03.2022г. №440 и от 01.04.2022г. №552.
4. Распоряжением Правительства РФ от 7 июня 2023г. №1495-р утверждена Стратегия развития фармацевтической промышленности на период до 2030 года, а от 9 сентября 2023г. №2436-р в рамках Сводной стратегии развития обрабатывающей промышленности РФ до 2024 года и на период до 2035 года утверждены Приоритетные направления развития фармацевтической и медицинской промышленности. В качестве ключевой цели развития отраслей Распоряжениями определено обеспечение на территории Российской Федерации производства качественных, эффективных и безопасных лекарств и медицинских изделий, обладающих конкурентоспособностью на внутренним и внешнем рынках, для удовлетворения потребности системы здравоохранения РФ и реализации экспортного потенциала, а целевыми показателями предусмотрено:
- увеличение объема внутреннего производства лекарственных средств до 808 млрд руб. к 2024г., до 1385 млрд руб. до 2030 года и до 1943 млрд руб. к 2035 году;
- увеличение производства медицинских изделий до 116 млрд руб. к 2024г., до 146 млрд руб. к 2030г. и до 150 млрд руб. к 2035 году.
5. Для достижения установленных постановлениями показателей, Минпромторг России по предложениям предприятий и организаций разработал и представил на съезде проект Плана мероприятий по реализации Стратегии развития фармацевтической промышленности, включающий весь комплекс вопросов, которые предстоит решить до 2030 года для создания конкурентоспособных лекарственных средств, в том числе низкомаржинальных, но востребованных отечественной системой здравоохранения:
- Совершенствование системы регулирования обращения лекарственных средств.
- Создание общей научно-исследовательской инфраструктуры в интересах отрасли.
- Подготовка научных, технологических и производственных кадров для фармацевтической промышленности.
- Обеспечение достаточным по номенклатуре и количеству исходным сырьем и материалами локального производства, прежде всего продукцией химического и биологического синтеза.
- Организация научной, производственной и технологической кооперации в смежных отраслях промышленности.
- Усовершенствование инструментов государственной поддержки финансового и регуляторного характера, стимулирующих развитие локального производства лекарств и компетенций для их разработки, как важнейшего фактора реализации государственной политики в сфере охраны здоровья граждан Российской Федерации.
6. В предложениях по реализации приоритетных направлений развития медицинской промышленности, представленных Союзом ассоциаций и предприятий медицинской промышленности, обращается внимание на необходимость усиления мер обеспечения локального производства востребованных медицинских изделий в объемах необходимых для удовлетворения потребности системы здравоохранения, повышения уровня технологической независимости производства продукции, развитие и поддержание научно-технологического, промышленного и кадрового потенциала на уровне, обеспечивающем выпуск высоко-технологичных, соответствующим мировым стандартам медицинских изделий с расширенной номенклатурой и использованием сырья, материалов, комплектующих и компонентной базы отечественного производства.
7. Анализ эффективности использования потенциала фармацевтической и медицинской промышленности показывает, что увеличение доли продукции отечественного производства на российском рынке и ускорение достижения технологического суверенитета, как комплекса мер, обеспечивающих использование имеющегося кадрового, финансового, технологического и материального ресурсов, в значительной мере по-прежнему сдерживается несовершенством существующей системы регулирования обращения лекарственных средств и медицинских изделий, непоследовательностью при применении государственной поддержки, закупках продукции для государственных и муниципальных нужд, государственной регистрации медицинских товаров и регулирования предельных отпускных цен производителей на них, недоработкой в оценке перспектив и стратегии развития отрасли. В результате, созданные в Российской Федерации мощности по выпуску современных высоко технологичных лекарственных средств и медицинских изделий используются не полностью. По-прежнему, нередко, при наличии доступных российских аналогов конкурентоспособная продукция закупается по импорту, что не создает достаточных стимулов к привлечению инвестиций в развитие фармацевтической и медицинской промышленности. В результате сохраняется зависимость здравоохранения страны от импорта, а государство теряет десятки миллиардов рублей при закупках импортной медицинской продукции.
В целях развития потенциала предприятий по производству лекарственных средств и медицинских изделий, усиления компетенций в освоении новых медицинских технологий за счет продукции отечественного производства и улучшения координации взаимодействия бизнеса и государства для достижения технологического суверенитета, съезд постановляет:
1. Одобрить проект Плана мероприятий по реализации Стратегии развития фармацевтической промышленности на период до 2030 года, представленный Минпромторгом России, и рекомендовать Правительству РФ утвердить План.
2. Принять за основу предложения Союза ассоциаций и предприятий фармацевтической и медицинской промышленности по реализации приоритетных направлений развития медицинской промышленности на период до 2030 года. Рекомендовать Ассоциации «Росмедпром» совместно с АНО «Консорциум «Медицинская Техника» разработать на его основе План развития медицинской промышленности до 2030 года, и после обсуждения профильными комиссиями и комитетами профессиональных общественных объединений, представить в Минпромторг России и в МВКС коллегии Военно-промышленной комиссии по развитию производства медицинских изделий в организациях ОПК.
3. Союзу ассоциаций и предприятий фармацевтической и медицинской промышленности разработать, согласовать с Минздравом России, Минпромторгом России и Росздравнадзором План мероприятий по реализации предложений, высказанных на съезде, предусматривающих достижение целевых показателей развития производства лекарственных средств и медицинских изделий до 2024 года, определенных распоряжением Правительства РФ от 09.09.2023г. №2436-р, предусмотреть в нём:
3.1. Проведение анализа существующих мер государственной поддержки производства продуктов малотоннажной химии для обеспечения потребностей фармацевтической и медицинской промышленности и разработку механизма возмещения, при котором производители лекарственных средств и медицинских изделий могут закупать отечественное сырьё и материалы по ценам конкурентоспособным с зарубежными.
3.2. Разработку инструментов прослеживаемости и оценки подтверждения фактора синтеза фармацевтической субстанции на территории Российской Федерации, оценку плана мероприятий по создания механизма подтверждения соответствия сведений о стадиях технологического процесса производства лекарственных средств, осуществляемых на территории РФ. Предложения по поддержке производства фармацевтических субстанций, интермедиатов и готовых лекарственных препаратов, локализуемых по полному циклу производства.
3.3. Утверждение методических рекомендаций по проведению экспертной оценки медицинской продукции на соответствие их критериям подтверждения производства на территории РФ, предусмотренных постановлением Правительства РФ от 17.07.2015 №719 с учетом особенностей подтверждения российского производства материалов, сырья и комплектующих, используемых в технологиях получения медицинской продукции, а также упрощенного порядка обновления актов экспертизы и заключения Минпроторга России при внесении изменений в регистрационные удостоверения, не оказывающих влияние на технологические процессы производства.
3.4. Приведение в соответствие с правом ЕАЭС, регулирующим обращение лекарственных средств для медицинского применения, положения о контроле качества одной серии каждого выпущенного в гражданский оборот лекарственного препарата, а также введение научного и предрегистрационного консультирования заявителей по вопросам процедур, связанных с регистрацией, экспертизой и испытанием лекарственных средств.
3.5. Внесение изменений в постановление Правительства РФ от 30.12.2015 №1517 в части совершенствования порядка перерегистрации предельных отпускных цен производителей на имплантируемые медицинские изделия, как было установлено п.8 постановления.
3.6. Мероприятия по совершенствованию организации государственного контроля и регистрации лекарственных средств и медицинских изделий с учетом разрабатываемой Правительством РФ Концепции контрольно-надзорной деятельности на период до 2026 года.
3.7. Вопросы повышения информативности КТРУ в отношении медицинских изделий, подлежащих регулированию в рамках режима закупок для государственных и муниципальных нужд.
3.8. Вопросы подготовки кадров и привлечения научно-технического персонала высшей школы и учреждений Минздрава России и РАН для фармацевтической и медицинской промышленности.
3.9. Исключение из статьи 238.1 УК РФ «медицинские изделия»
4. Рекомендовать Минпромторгу России и Росздравнадзору:
- Ускорить представление в Правительство РФ проектов постановлений Правительства РФ «Об утверждении правил государственной регистрации медицинских изделий», «О внесении изменений в постановление Правительства РФ «Об утверждении положения о лицензировании деятельности по техническому обслуживанию медицинских изделий…», «О государственном регулировании цен на медицинские изделия, включенные в перечень медицинских изделий, имплантируемых в организм человека…, «О проведении эксперимента по созданию системы прослеживаемости технологического процесса производства лекарственных средств» и в постановление Правительства РФ о государственном регулировании цен на ЖНВЛП.
- Провести актуализацию образовательных стандартов и программ подготовки кадров для фармацевтической и медицинской промышленности с учетом современного уровня развития науки и технологий в сфере здравоохранения.
- Разработать дополнительные меры по поддержке производителей лекарственных препаратов и медицинских изделий при продвижении продукции на внешние рынки, в том числе, в соответствии с поручением Президента РФ от 04.06.2023г. №Пр-1118ГС разработать проект постановления Правительства РФ по изменению условий доступа продукции иностранного производства, которая локализована в РФ в объемах, достаточных для удовлетворения внутреннего спроса.
- Представить в Правительство РФ законопроект о внесении изменений в Налоговый кодекс в части снижения размера пошлин за внесение изменений в регистрационные досье на лекарственные препараты.
- Повысить активность торговых представительств по оказанию помощи российским производителям лекарственных средств и медицинских изделий в поиске зарубежных партнеров для сотрудничества, регистрации продукции и продвижению её на внешние рынки.
- Определить плановую потребность в обновлении медицинского оборудования лечебно-профилактических учреждений федерального и регионального уровней и довести её до Союза ассоциаций и предприятий фармацевтической и медицинской промышленности.
- Уточнить центры компетенции по развитию производства лекарственных средств и медицинских изделий, не производимых в РФ, предусмотрев для них специальные меры государственной поддержки и увязав их с работой научно-образовательных комплексов полного цикла Минздрава России.
5. Просить Правительство Российской Федерации:
- дополнительно рассмотреть предложения профессиональных общественных объединений по уточнению государственных пошлин за совершение действий уполномоченным органом исполнительной власти при осуществлении государственной регистрации лекарственных средств;
- исключить продукцию фармацевтической отрасли из-под действия требований постановления Правительства РФ от 21.09.2023 №1538 об уплате экспортных пошлин;
- внедрить научное и предрегистрационное консультирование заявителей по вопросам процедур, связанных с регистрацией, экспертизой и испытанием лекарственных средств;
- поддержать предложения предприятий медицинской и фармацевтической промышленности не вводить акциз на спирт этиловый, используемый в производстве лекарственных средств и медицинских изделий, так как введение акциза не решит проблему фальсифицированной продукции, а сделает производство медицинской продукции экономически нецелесообразным, из-за того, что этиловый спирт является основным растворителем, применяемой в технологии синтеза большого количества лекарственных средств и медицинских изделий.